O que é?
Car T cell significa Células T com receptores de antígeno quimérico. É uma terapia celular inovadora no combate ao câncer.
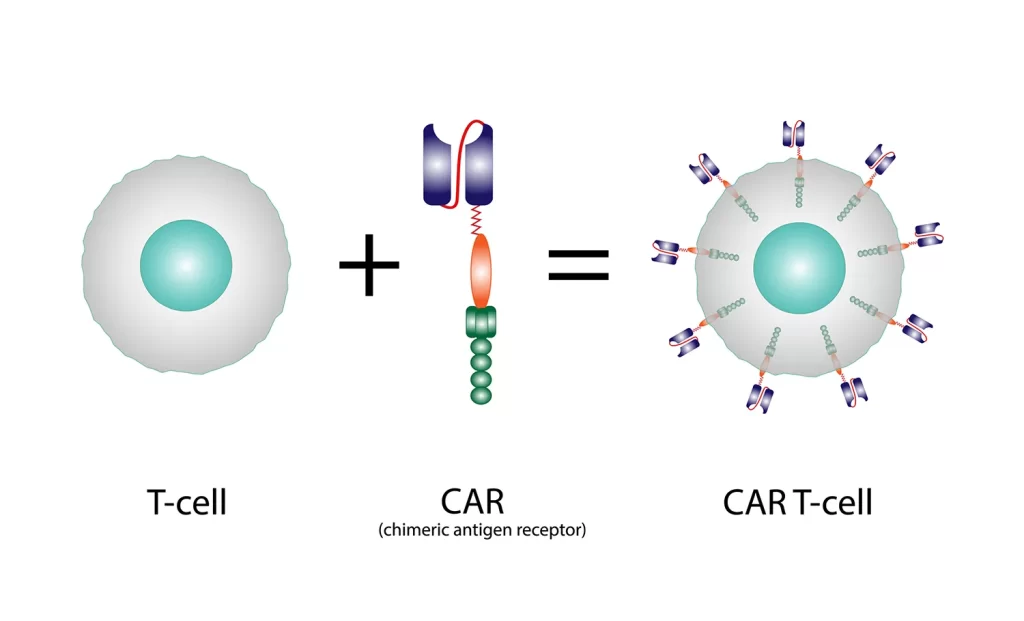
Como é feita?
Primeiro ponto é Identificar o paciente candidato a terapia (Pacientes com LLA B, LDGCB, LCM ou MM). Depois é feita a coleta dos linfócitos por leucaférese, sendo a célula encaminhada para o laboratório para a inserção do receptor quimérico. O Receptor quimérico é resultado de uma fusão de um domínio de um anticorpo e porções de receptor de células T.
A porção FAB do anticorpo que é responsável pelo reconhecimento do antígeno (alvos na célula do câncer, ex: CD 19 e BCMA) + alça extracelular e transmembrana + porção intracelular (TCR CD3 [CD3-zeta]) responsável por ativar os linfócitos T que carregam o CAR.
Essa porção intracelular pode conter diversas moléculas estimuladores e coestimuladores e isso é a diferença entre as gerações das CAR-T cels. As primeiras gerações só tinham moléculas envolvidas no sinal 1 de estimulação do linfócito T em comparação os de 3 geração possuem dois fatores a mais de coestimulação
Esse receptor quimérico é inserido na membrana celular através de um vetor (ex viral) que insere o código genético do CAR no material genético do linfócito, resultando na transcrição do CAR e sua expressão na membrana.
Depois é feita a expansão ex vivo das as células CAR-T (10 a 20 dias) e, então, as Car T cel podem ser infundidas no paciente.
Uma vez na circulação do paciente as car T cell vão reconhecer um antígeno específico da superfície tumoral/celular o que ativa a resposta das células T.
Os efeitos colaterais das células CAR-T
- Síndrome de liberação de citocinas (SIRS): febre, hipotensão, alteração do estado mental e convulsões. Tocilizumab e corticoide.
- Síndrome de neurotoxicidade associada a células efetoras imunes (ICANS), uma síndrome neuropsiquiátrica. Corticoide e anticonvulsivantes
- Citopenias e infecções.
Produtos registrados pela ANVISA
- Kymriah (tisagenlecleucel): Leucemia linfoblástica aguda (LLA) de células B e linfoma difuso de grandes células B.
- Carvykti (ciltacabtageno autoleucel): Mieloma múltiplo
- Yescarta® (axicabtagene ciloleucel): Linfoma de Grandes Células B (LDGCB), recidivado ou refratário, após duas ou mais linhas de terapia sistêmica
- TECARTUS® (Brexucabtagene autoleucel): linfoma de células do manto (LCM) e leucemia linfoblástica aguda (LLA),
Linha Temporal:
- 23/02/2022 - Ocorreu o primeiro registro sanitário para produto de terapia gênica com células CAR-T para tratamento de câncer hematológico.
O Kymriah® é indicado para o tratamento de pacientes até 25 anos de idade LLA B, refratária ou a partir da segunda recidiva e para pacientes adultos com LDGCB recidivado ou refratário, após duas ou mais linhas de terapia sistêmica.
Estudo ELIANA: 75 pacientes de até 25 anos com LLA-B. OS de 76% em 12 meses.
Estudo JULIET: paciente com linfomas de grandes células B R/R: sobrevida livre de recidiva de 65% em 12 meses.
- 01/04/2022 - Segundo car T cell aprovado.
Carvykti® (ciltacabtageno autoleucel / Cilta-cel) para pacientes com mieloma múltiplo que não responderam ao tratamento com as três classes (agentes imunomoduladores, inibidores de proteassoma e anticorpos monoclonais)
Estudos
CARTITUDE-1: pacientes com MM R/R (incluindo um agente imunomodulador, um inibidor de proteassoma e um anticorpo monoclonal CD38 como parte das quatro ou mais linhas): ORR foi de 97% e a OS em 12 meses foi de 89%,
CARTITUDE-4 avaliou o cilta-cel em comparação com o tratamento padrão na segunda linha em pacientes refratários à lenalidomida. After a median follow-up of 15.9 months, cilta-cel resulted in deeper responses and superior PFS (12-month PFS 76 versus 49 percent; HR 0.26, 95% CI 0.18-0.38). OS data are immature.
- 26/10/2022 - Aprovado o registro sanitário de mais um produto de terapia à base de células modificadas geneticamente para tratamento do câncer.
Yescarta® (axicabtagene ciloleucel / axi-cel) para pacientes adultos com Linfoma de Grandes Células B (LDGCB), recidivado ou refratário, após duas ou mais linhas de terapia sistêmica.
Estudos:
ZUMA-7 comparou o uso de axi-cel ao transplante autólogo de células-tronco (TASC) em pacientes com LDGCB refratário primário ou com LDGCB que recidiva dentro de 12 meses do tratamento inicial.
Com uma mediana de seguimento de 47 meses, os paciente submetidos ao tratamento com axicabtagene ciloleucel tiveram maior sobrevida global em 4 anos (OS; 55% x 46 %; hazard ratio [HR] 0.73 [95% CI 0.54-0.98]) e, também , maior sobrevida livre de progressão (PFS; 42 % x 24%; HR 0.51 [95% CI 0.38-0.67]).
- 29/12/2023 - Mais um produto de terapia gênica que utiliza as células T foi aprovado.
Brexucabtagene autoleucel / Brexu-cel / TECARTUS®: para adultos com linfoma de células do manto (LCM) após dois ou mais tratamentos anteriores el para o tratamento de leucemia linfoblástica aguda (LLA) recorrente ou sem resposta às terapias anteriores.
Estudos:
ZUMA-2: pacientes LCM refratários a três ou mais linhas de terapia anteriores e todos haviam recebido um inibidor de tirosina quinase de Bruton (BTKi) anteriormente. Sobrevida global estimada em 12 meses foi de 83%
Estudo ZUMA-3: LLA B 56% de resposta completa. Mediana de sobrevida global de mais de 18 meses.
